Krystalizator laboratoryjny to specjalistyczne naczynie, którego konstrukcja i przeznaczenie są ściśle związane z procesami wymagającymi precyzyjnego odparowywania rozpuszczalnika. Jego kluczowa rola w wielu procesach chemicznych, takich jak krystalizacja czy oczyszczanie substancji, sprawia, że jest nieodzownym elementem wyposażenia każdego laboratorium. W tym artykule przyjrzymy się bliżej jego funkcjom, budowie i wszechstronnym zastosowaniom, aby w pełni zrozumieć jego znaczenie.
Krystalizator laboratoryjny służy do kontrolowanej krystalizacji, oczyszczania i zagęszczania roztworów
- Jest to naczynie laboratoryjne o płaskim dnie i dużej powierzchni parowania.
- Służy przede wszystkim do kontrolowanej krystalizacji i otrzymywania czystych kryształów.
- Wykorzystywany jest również do oczyszczania związków chemicznych i zagęszczania roztworów.
- Wykonany ze szkła borokrzemowego lub porcelany, co zapewnia odporność chemiczną i termiczną.
- Jego konstrukcja sprzyja powolnemu odparowywaniu rozpuszczalnika dla uzyskania idealnych kryształów.
Krystalizator w laboratorium: czym właściwie jest i dlaczego jego rola jest kluczowa?
Definicja krystalizatora: więcej niż zwykłe naczynie laboratoryjne
Krystalizator to naczynie laboratoryjne o charakterystycznym, zazwyczaj cylindrycznym kształcie i płaskim dnie. Został on zaprojektowany w taki sposób, aby maksymalizować powierzchnię kontaktu cieczy z otaczającym powietrzem, co jest kluczowe dla procesu powolnego odparowywania. Jego głównym zadaniem jest wspomaganie procesu krystalizacji czyli kontrolowanego wytrącania kryształów substancji stałej z roztworu. Nie jest to zwykłe naczynie, ale precyzyjne narzędzie, które odgrywa fundamentalną rolę w wielu procesach laboratoryjnych.Charakterystyczna budowa: dlaczego płaskie dno i duża średnica mają znaczenie?
Kluczowe cechy konstrukcyjne krystalizatora to jego płaskie dno oraz duża średnica w stosunku do wysokości. Taka budowa, zapewniająca znaczną powierzchnię parowania, jest niezbędna do tego, aby rozpuszczalnik mógł odparowywać w sposób powolny i kontrolowany. To właśnie ta cecha sprawia, że krystalizator jest idealnym naczyniem do uzyskiwania dużych, dobrze uformowanych i czystych kryształów. Im większa powierzchnia parowania, tym efektywniejsze jest usuwanie rozpuszczalnika, co bezpośrednio przekłada się na jakość otrzymywanych kryształów.
Krystalizator a inne szkło laboratoryjne: czym różni się od zlewki, parownicy i szalki Petriego?
W świecie szkła laboratoryjnego krystalizator zajmuje unikalne miejsce. Różni się znacząco od innych popularnych naczyń. Zlewka, choć również posiada płaskie dno, jest przede wszystkim przeznaczona do przechowywania, mieszania i podgrzewania substancji, a jej konstrukcja nie sprzyja kontrolowanemu odparowywaniu. Parownica, z kolei, charakteryzuje się szerokim, płytkim kształtem, ale jej celem jest szybkie odparowanie rozpuszczalnika, co często prowadzi do powstania drobnego osadu lub proszku. Szalka Petriego jest płytka i szeroka, służąc głównie do hodowli mikroorganizmów lub przechowywania niewielkich próbek. Krystalizator natomiast, dzięki swojej specyficznej proporcji średnicy do wysokości, optymalizuje proces powolnego odparowywania, co jest kluczowe dla otrzymywania wysokiej jakości kryształów, a nie szybkiego odparowania czy hodowli.
Główne zadanie: jak krystalizator wspiera proces powstawania idealnych kryształów?
Krystalizacja krok po kroku: od nasyconego roztworu do czystej substancji
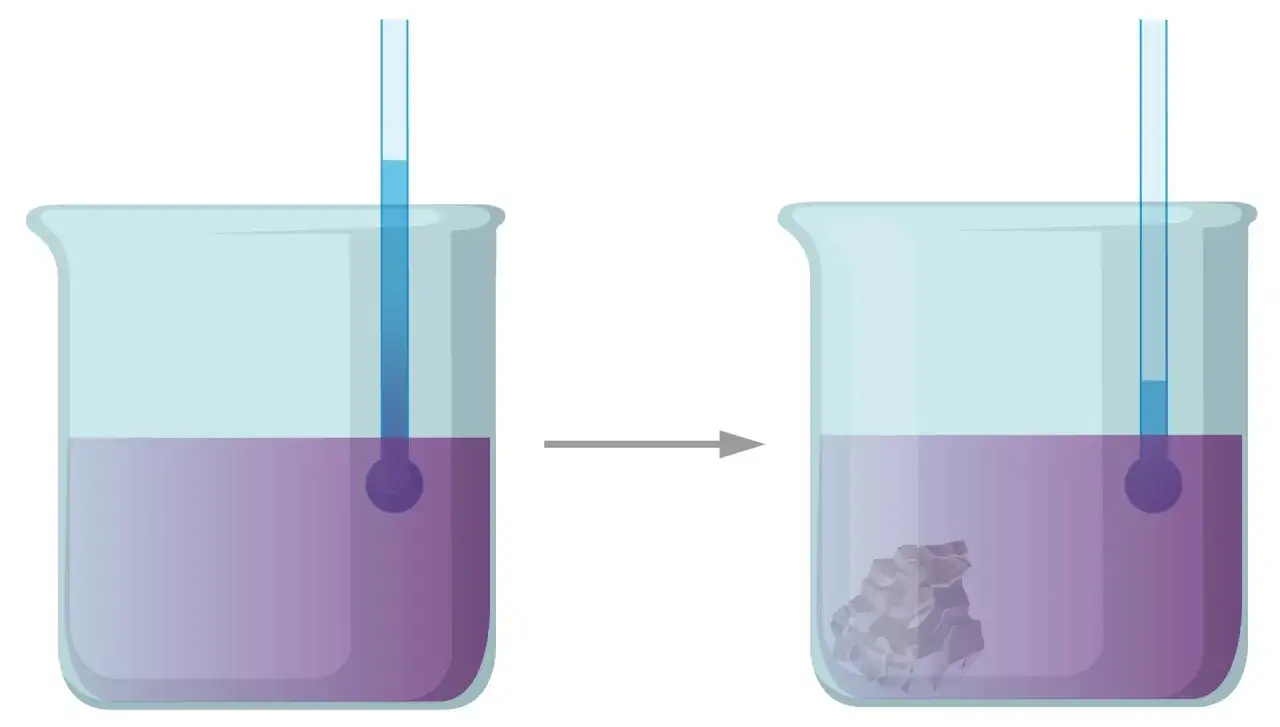
Proces krystalizacji w krystalizatorze rozpoczyna się od przygotowania roztworu nasyconego, czyli takiego, w którym rozpuszczono maksymalną możliwą ilość substancji w danej temperaturze. Następnie, poprzez powolne odparowywanie rozpuszczalnika, roztwór staje się przesyccony przekracza granicę rozpuszczalności. W tym momencie zaczynają tworzyć się pierwsze zarodki krystaliczne, które następnie rosną. Jak podaje Danlab, krystalizacja jest procesem, który pozwala na uzyskanie substancji w stanie stałym o wysokim stopniu czystości, co jest kluczowe w wielu zastosowaniach. Krystalizator zapewnia idealne warunki do tego, by ten wzrost był kontrolowany i uporządkowany.
Rola powolnego parowania: sekret uzyskiwania dużych i regularnych struktur krystalicznych
Powolne parowanie rozpuszczalnika to serce procesu krystalizacji w krystalizatorze. Ta metoda pozwala cząsteczkom substancji rozpuszczonej na stopniowe i uporządkowane układanie się w sieć krystaliczną. Dzięki temu procesowi powstają większe, bardziej regularne i czystsze kryształy. Szybkie odparowanie, które mogłoby zajść w innych naczyniach, prowadziłoby do chaotycznego wytrącania się cząsteczek, skutkując powstawaniem małych, często zanieczyszczonych kryształów lub nawet amorficznych osadów, które nie posiadają uporządkowanej struktury.
Czynniki wpływające na sukces krystalizacji w krystalizatorze
Sukces procesu krystalizacji w krystalizatorze zależy od kilku kluczowych czynników. Niezwykle ważna jest kontrola temperatury jej stabilność sprzyja powstawaniu jednolitych kryształów. Równie istotna jest czystość rozpuszczalnika, która zapobiega wprowadzaniu dodatkowych zanieczyszczeń. Stopień nasycenia roztworu musi być odpowiednio dobrany, aby zainicjować krystalizację, ale nie doprowadzić do zbyt szybkiego wytrącania. Wreszcie, obecność zarodków krystalizacji, czyli małych kryształków, może przyspieszyć i ukierunkować proces wzrostu. Konstrukcja krystalizatora, ze swoją dużą powierzchnią parowania, ułatwia zarządzanie tymi czynnikami, zapewniając optymalne warunki.
Nie tylko krystalizacja: poznaj wszechstronne zastosowania krystalizatora
Oczyszczanie związków chemicznych: jak oddzielić zanieczyszczenia od pożądanego produktu?
Krystalizacja jest jedną z najskuteczniejszych i najczęściej stosowanych metod oczyszczania związków chemicznych w chemii analitycznej i preparatywnej. Krystalizator odgrywa tu kluczową rolę. Podczas gdy pożądana substancja tworzy dobrze uformowane kryształy, większość zanieczyszczeń, które mają inną rozpuszczalność lub po prostu nie krystalizują w danych warunkach, pozostaje w roztworze macierzystym. Następnie, poprzez filtrację, można łatwo oddzielić czyste kryształy od cieczy zawierającej zanieczyszczenia. Krystalizator umożliwia precyzyjne przeprowadzenie tego procesu.
Zagęszczanie roztworów: kiedy i dlaczego warto odparować nadmiar rozpuszczalnika?
Dzięki swojej konstrukcji, zapewniającej dużą powierzchnię parowania, krystalizator jest również doskonałym narzędziem do zagęszczania roztworów. Proces ten polega na efektywnym usuwaniu nadmiaru rozpuszczalnika, co prowadzi do zwiększenia stężenia substancji rozpuszczonej. Zagęszczanie roztworów może być konieczne przed dalszymi etapami analiz, reakcjami chemicznymi, a także w celu zwiększenia wydajności procesu krystalizacji poprzez doprowadzenie do wyższego stopnia przesycenia. Krystalizator pozwala na kontrolowane zagęszczanie, minimalizując ryzyko wytrącenia się niepożądanych produktów ubocznych.
Inne praktyczne funkcje: suszenie osadów i przechowywanie próbek
Wszechstronność krystalizatora nie kończy się na krystalizacji i zagęszczaniu. Jego płaskie dno i duża powierzchnia sprawiają, że jest on również przydatny do suszenia niewielkich ilości osadów chemicznych. Rozłożony na płasko materiał szybciej oddaje wilgoć. Ponadto, krystalizator może służyć jako naczynie do tymczasowego przechowywania próbek, zwłaszcza tych, które wymagają kontaktu z powietrzem lub stabilnej, płaskiej powierzchni. Jest to więc naczynie o wielu zastosowaniach, które znajduje swoje miejsce w różnorodnych procedurach laboratoryjnych.
Z czego wykonany jest profesjonalny krystalizator i dlaczego ma to znaczenie?
Szkło borokrzemowe (BORO 3.3): złoty standard w odporności chemicznej i termicznej
Najczęściej krystalizatory wykonuje się ze szkła borokrzemowego, często oznaczonego jako BORO 3.3 lub Duran. Jest to materiał o wyjątkowych właściwościach, ceniony w laboratoriach za swoją wysoką odporność na działanie szerokiej gamy chemikaliów, w tym stężonych kwasów i zasad. Ponadto, szkło borokrzemowe charakteryzuje się doskonałą odpornością na szok termiczny, czyli gwałtowne zmiany temperatury, co jest kluczowe w procesach laboratoryjnych, gdzie często dochodzi do ogrzewania lub chłodzenia naczyń. Przezroczystość i obojętność chemiczna tego materiału zapewniają bezpieczeństwo i precyzję eksperymentów. Jak podaje Danlab, materiały takie jak szkło borokrzemowe są preferowane ze względu na ich stabilność chemiczną i termiczną.
Krystalizatory porcelanowe: kiedy warto po nie sięgnąć?
Alternatywą dla szkła borokrzemowego są krystalizatory wykonane z porcelany. Są one często wybierane ze względu na swoją większą wytrzymałość mechaniczną w porównaniu do szkła, co czyni je bardziej odpornymi na stłuczenia. Porcelana pozwala również na pracę w wyższych temperaturach. Choć nieprzezroczystość porcelany może być wadą w niektórych zastosowaniach, gdzie obserwacja procesu jest kluczowa, w innych przypadkach może stanowić zaletę, na przykład chroniąc zawartość przed światłem. Krystalizatory porcelanowe są często stosowane w procesach wymagających większej odporności mechanicznej lub termicznej.
Konstrukcyjne detale, które ułatwiają pracę: znaczenie wylewu i wzmocnionego obrzeża
Oprócz podstawowej budowy, profesjonalne krystalizatory często wyposażone są w drobne, ale znaczące detale konstrukcyjne. Wylew, czyli tzw. „dzióbek”, ułatwia precyzyjne przelewanie cieczy i minimalizuje ryzyko rozlania, co jest szczególnie ważne przy pracy z cennymi lub niebezpiecznymi substancjami. Wzmocnione obrzeże krystalizatora zwiększa jego trwałość, chroni przed uszkodzeniami mechanicznymi podczas manipulacji oraz zapewnia pewniejszy chwyt. Te pozornie niewielkie udogodnienia znacząco wpływają na komfort i bezpieczeństwo pracy w laboratorium.
Jak prawidłowo wybrać i użytkować krystalizator, by służył latami?
Dobór rozmiaru i pojemności do skali eksperymentu: na co zwrócić uwagę?
Wybór odpowiedniego rozmiaru i pojemności krystalizatora jest kluczowy dla sukcesu eksperymentu. Należy go dopasować do skali planowanych prac czy jest to analiza niewielkiej ilości substancji, czy synteza na większą skalę. Ważne jest, aby objętość roztworu nie przekraczała optymalnego poziomu, który zapewni odpowiednią powierzchnię parowania. Krystalizatory dostępne są w szerokim zakresie pojemności, od kilkudziesięciu mililitrów do kilku litrów. Zbyt małe naczynie może prowadzić do zbyt szybkiego odparowania, a zbyt duże do nieefektywnego procesu, jeśli objętość roztworu jest niewielka.
Najczęstsze błędy podczas pracy z krystalizatorem i jak ich unikać
Podczas pracy z krystalizatorem można popełnić kilka typowych błędów. Jednym z nich jest zbyt szybkie odparowywanie, wynikające na przykład z umieszczenia naczynia w zbyt ciepłym miejscu lub na bezpośrednim słońcu, co prowadzi do powstania drobnych, niejednorodnych kryształów. Kolejnym problemem jest zanieczyszczenie roztworu należy dbać o czystość otoczenia i używać czystych narzędzi. Niewłaściwy dobór materiału krystalizatora do substancji chemicznej może prowadzić do niepożądanych reakcji. Aby tego uniknąć, zawsze należy dokładnie zapoznać się z właściwościami substancji i dobrać odpowiednie naczynie. Unikaj również gwałtownych zmian temperatury, które mogą spowodować pęknięcie szkła.
Przeczytaj również: ALAB wyniki: Jak szybko je otrzymasz i sprawdzisz online?
Praktyczne wskazówki dotyczące czyszczenia i konserwacji szkła laboratoryjnego
Aby krystalizatory i inne szkło laboratoryjne służyły długo i niezawodnie, należy o nie odpowiednio dbać. Po każdym użyciu naczynia należy dokładnie umyć, najlepiej przy użyciu łagodnych detergentów laboratoryjnych. Należy unikać stosowania środków ściernych lub druciaków, które mogą porysować powierzchnię szkła. Po umyciu szkło należy dokładnie wypłukać wodą destylowaną, aby usunąć wszelkie pozostałości detergentu. Następnie naczynia należy osuszyć, najlepiej na powietrzu na stojaku do suszenia lub w suszarce laboratoryjnej. Prawidłowa konserwacja i przechowywanie w bezpiecznym miejscu zapobiegają kontaminacji i przedłużają żywotność sprzętu, zapewniając jego gotowość do kolejnych eksperymentów.